(간호연구) 윤리
윤리의 역사적 배경
미국
1932~1972년까지 매독을 치료하지 않았을 때의 자연적인 질병 경과를 알기 위하여 400명 이상의 앨라바마 흑인 소작농과 노무자를 대상으로 한 연구

1963년 브루클린의 유태인 만성질환 병원
인체의 거부반응을 알아보고자 노인 입원 환자에게 알리지도 않고 살아 있는 암세포를 주사한 연구가 있었다.

펜실베니아의 주립정신병원(pennsylvaniastate hospital)
수용된 환자에게 폐렴, 독감, 뇌막염을 실험하였다. 이와 같이 가난하고 무지한 사람을 대상으로 연구를 수행한 역사가 많다.

독일
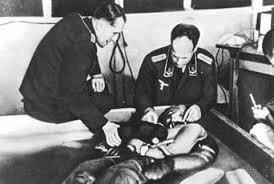
나치는 전쟁포로 · 불구자 · 정신이상자 · 노인 · 순수 아리안족이 아닌 사람들에게 생체 의학실험

일본
‘관동군731부대’에서 전쟁포로(주로 한국인, 중국인, 만주인, 러시아인 등)를 실험 대상자인 마루타(껍데기만 벗긴 통나무라는 뜻의 일본어)라고 부르며 생체실험용으로 이용하였다.
대상자들을 아무런 보호장비 없이 높은 고도, 영하의 추운날씨에 노출시켜 인간의 생체반응을 조사하거나, 말라리아나 장티프스균 · 독극물 · 검증되지 않은 약 등을 주입하여 반응을 보고 건강한 사람에게로 전염병이 퍼지는 속도를 조사하였으며, 마취 없는 수술이 가능한지 등의 인간의 한계와 반응을 연구하였다.


1949년 뉴렘베르그 강령(Nuremberg code)
제2차 세계대전이 끝나고 뉴렘베르그 군사재판 이후 인간 대상자를 위한 공식적 윤리표준을 설정


자발적 동의, 연구에서 대상자 참여 중단, 신체적 정신적 고통과 손상, 불구, 죽음 등으로부터 대상자 보호, 그리고 연구로 인한 이득과 위험의 균형에 대한 지침이 포함되어 있으며, 모든 경우에 사전동의를 요구하고 어린이, 노인, 정신장애자에게 어떠한 특별한 처치도 행하지 못하도록 하였다.
뉴렘베르그 강령은 헬싱키 선언의 기초
Nuremberg code
- Required is the voluntary, well-informed, understanding consent of the human subject in a full legal capacity.
→ 법적 능력을 갖춘 연구 대상자의 자발적이고 충분히 이해된 동의는 필수적이다. - The experiment should aim at positive results for society that cannot be procured in some other way.
→ 실험은 다른 방법으로는 얻을 수 없는 사회적 유익한 결과를 목표로 해야 한다. - It should be based on previous knowledge (like, an expectation derived from animal experiments) that justifies the experiment.
→ 실험은 기존 지식(예: 동물실험에서 도출된 결과 등)에 근거하여 정당화되어야 한다. - The experiment should be set up in a way that avoids unnecessary physical and mental suffering and injuries.
→ 실험은 불필요한 신체적 · 정신적 고통과 손상을 피하도록 설계되어야 한다. - It should not be conducted when there is any reason to believe that it implies a risk of death or disabling injury.
→ 사망이나 장애를 초래할 위험이 있다고 판단될 경우 실험을 수행해서는 안 된다. - The risks of the experiment should be in proportion to (that is, not exceed) the expected humanitarian benefits.
→ 실험의 위험성은 기대되는 인도주의적 이익을 초과해서는 안 된다. - Preparations and facilities must be provided that adequately protect the subjects against the experiment’s risks.
→ 연구 대상자를 위험으로부터 충분히 보호할 수 있는 준비와 시설이 제공되어야 한다. - The staff who conduct or take part in the experiment must be fully trained and scientifically qualified.
→ 실험을 수행하거나 참여하는 연구진은 충분한 훈련과 과학적 자격을 갖추어야 한다. - The human subjects must be free to immediately quit the experiment at any point when they feel physically or mentally unable to go on.
→ 연구 대상자는 신체적·정신적으로 더 이상 실험을 지속할 수 없다고 느끼는 경우 언제든지 즉시 중단할 자유가 있다. - Likewise, the medical staff must stop the experiment at any point when they observe that continuation would be dangerous.
→ 또한 연구진은 실험의 지속이 위험하다고 판단될 경우 언제든지 실험을 중단해야 한다.
헬싱키 선언
헬싱키 선언은 세계의사회(World Medical Association)에서 1964년 채택 – 세계의사협회총회에서 채택된 의료 윤리 선언
2008년 개정된 헬싱키 선언문의 한국어 번역본은 대한의사협회지에서 찾아볼 수 있다
(http://ocr.yuhs.ac/MDCTC/UploadZone/Files/Common/Declaration_Of_Helsinki_ko_2008_seoul.pdf).
뉴렘베르그 강령과 헬싱키 선언이 연구에서의 윤리성에 기준을 제공하였다.

벨몬트 보고서
1974년 미국의회 – 생의학 · 행동연구에서 인간 대상자 보호를 위한 국가위원회(The National Commission for Protection of Human Subjects of Biomedical and Behavioral Research)가 구성
– 1979년 벨몬트 보고서(Belmont Report)출판
U.S. Department of Health & Human Services 홈페이지에서 검색이 가능하다.
(http://www.hhs.gov/ohrp/humansubjects/guidance/belmont.html)
인간 대상자 보호를 위한 윤리원칙
선행
연구자는 대상자의 이득은 최대화하고, 신체적 · 정서적 · 사회적 손상 등 해는 최소화해야 한다.
인간존중
대상자의 자기결정권과 알 권리를 보장하며, 자율성이 부족한 취약 대상자는 특별히 보호해야 한다.
정의
연구의 이득과 부담을 공평하게 분배하고 대상자의 사생활과 정보를 철저히 보호해야 한다.
취약한 대상자(Vulnerable Subjects)
정의 : 자율성이 떨어지거나 연구 참여 결정에 영향을 받을 수 있어 특별 보호가 필요한 대상자
| 유형 | 특성 및 보호 원칙 |
| 어린이, 무의식 환자, 인지장애자 | 위험 평가 능력 부족 → 법적 대리인(부모 · 보호자) 동의 필수 |
| 죄수 | 자유 의사 제한, 형기감소 · 금전 등이 부당한 동기 될 수 있음 |
| 학생 | 연구 참여 여부가 성적 · 추천서에 영향 없어야 함 |
| 고용인 | 연구 참여가 승진 · 보수 · 지위와 무관해야 함 |
| 기타 특별 고려 대상 | 노인, 임종환자, 입원환자, 노숙자, 성전환자 등 |
인간 대상자를 위한 윤리적 보호 방법
사전동의
대상자는 연구내용을 충분히 숙지하고 자발적으로 참여을 결정 해야 하며, 질적연구에서는 진행 과정에 따라 지속적인 재동의 과정이 필요하다/
연구윤리 심의위원회
IRB
대상자의 윤리적 보호를 위해 기관내에 설치된 독립적 심의기구로 연구계획서 검토, 승인, 수정요구, 중지 권한을 가지며 다양한 분야의 전문가와 외부인사로 구성된다.
익명서, 비밀보장
연구자가 대상자의 신원을 전혀 알 수 없도록 하는 완전한 정보 차단
비밀보장 : 대상자의 신원은 알지만 연구지가 수집된 개인정보를 외부에 공개하지 않겠다는 약속
IRB
Institutional Review Board
기관생명윤리위원회(또는 기관윤리심의위원회)
2008년: 보건복지부, 기관생명윤리심의위원회 구성 · 운영 표준지침서 제작 · 배포
생명윤리 및 안전에 관한 법률제정으로 법적 기반 마련
2013년부터 : 인간 대상 연구 수행 기관(교육 · 연구기관, 병원)의 기관생명윤리위원회(IRB) 설치 의무화
관련 기관 및 정보
IRB 정보 포털 : http://www.irb.or.kr(보건복지부 지정)
KAIRB(대한기관윤리심의기구협의회) : http://www.kairb.org
IRB의 역할 : 인간 대상 연구의 윤리적 · 과학적 타당성 검토, 연구대상자 보호, 연구 진행 승인 및 관리
인권을 무시한 임상 연구 (피험자 보호의 실패)
터스키기 매독 연구 (Tuskegee Syphilis Study, 1932~1972)
연구윤리 위반 사건의 대명사로 꼽힌다. 미국 공중보건국이 흑인 남성 600여 명을 대상으로 진행한 이 연구에서, 연구자들은 참가자들에게 매독 진실을 숨기고 “나쁜 피(bad blood)” 치료를 빌미로 참여시켰다. 결정적으로 1940년대에 치료제인 페니실린이 개발된 후에도 이를 고의로 제공하지 않아 참가자들이 불필요한 고통과 사망에 이르게 했다. 이 사건은 1972년 폭로된 후 미국 사회에 큰 충격을 주었고, 1979년 벨몬트 보고서(Belmont Report) 발표와 연구윤리 심의위원회(IRB) 제도화의 직접적인 계기가 되었다.
윌로우브룩 간염 연구 (WillowbrookHepatitis Study, 1956~1970)
뉴욕의 윌로우브룩 주립학교에서 진행된 이 연구는 지적 장애가 있는 아동들을 대상으로 고의로 간염 바이러스에 감염시켜 질병의 진행 과정을 관찰했다. 부모님의 동의가 있었다 하더라도, 열악한 시설 환경에서 치료를 받기 위해 연구 참여가 사실상 강요된 측면이 있어, 취약한 집단을 대상으로 한 연구의 윤리적 문제를 극명하게 보여줬다.
과학적 진실을 훼손한 연구 부정행위
앤드루 웨이크필드의 백신-자폐증 연계 논문 (1998)
영국의 의사 웨이크필드는 논문을 통해 MMR(홍역 · 볼거리 · 풍진) 백신과 자폐증의 연관성을 주장했으나, 이는 의도적으로 데이터를 조작한 명백한 연구 부정행위였다. 이후 논문은 철회되었고 그의 면허도 취소되었지만, 이 사건은 전 세계적으로 백신에 대한 불신을 퍼뜨리고 ‘백신 회피’ 현상을 초래하여 공중보건에 막대한 피해를 남겼다.
황우석 사건 (2005)
대한민국 국민들에게 큰 충격을 안긴 이 사건은 생명공학 분야의 대표적인 논문 조작 사례다. 줄기세포 연구의 세계적 권위자로 추앙받던 황우석 박사팀의 연구 성과가 데이터 조작으로 밝혀지면서 과학계는 물론 사회 전체에 큰 파장을 일으켰다.
소보카타 하루코의 STAP 세포 논문 (2014)
일본의 젊은 연구자 소보카타 하루코가 발표한 혁신적인 줄기세포 연구(STAP 세포)는 데이터 조작과 표절 등 심각한 연구 부정행위로 밝혀져 Nature 논문이 철회되었다. 이 사건은 일본 과학계의 연구윤리 시스템 전반에 대한 반성과 제도 개혁을 이끌어냈다.
연구부정 행위
과학적 객관성
수집된 자료조작
연구자의 기대로 결과를 유도하는 행위
부정직한 행위
연구부정 행위
날조 : 존재하지 않은 데이터나 결과를 거짓으로 만들어 보고, 기록
변조 : 연구자료, 장비, 과정을 인위적으로 변경하거나 결과를 왜곡, 누락
표절 : 타인의 아이디어를 과정 결과 문구를 출처없이 도용
출판윤리
논문의 저자는 연구 기여도에 따라 제1저자. 교신저자. 공동저자로 구분되며. 실질적인 학술적인 기여를 한 사람에게 공정하게 배분되어야 한다.
연구윤리문제
선물 저자 : 기여 없는 사람을 예우나 관계로 저자에 포함
압력에 위한 저자 : 상급자가 기여없이 이름요구
명예저자 : 유명 인사 무단 등재
유령저자 : 실제기여 했으나 논문에서 제외
상호저자 : 논문에 넣어주기로 약속 거래
표절의 종류
단순표절
타인의 글을 적절한 인용없이 사용하는 행위
그대로 인용
바꿔쓰기
요약
자기표절
이미 출간된 자신의 글을 인용 없이 사용하는 행위
중복게제
자기표절의 한 유형
이미 공포된 자신의 논문을 또 다른 논문으로 다시 출간 하는 행위
KCI 문헌 유사도 검사 서비스
사이트 주소 : https://check.kci.go.kr/
운영 기관 : 한국연구재단 (National Research Foundation of Korea)
제1저자와 교신저자 , 공동저자
| 구분 | 역할 및 특징 |
| 제1저자 (First Author) | 저자 중 가장 앞에 배치, 연구 개념·설계, 자료수집·해석, 초안 작성에 가장 기여도가 큰 사람. 연구책임자(PI)가 주로 제1저자 역할 |
| 교신저자 (Corresponding Author) | 논문 출판 과정 전반(심사, 수정, 편집)을 책임지고 외부와 소통하는 저자 |
| 공동저자 (Co-author) | 연구에 의미 있는 학술적 기여를 한 공동 연구자 |
이해관계(Conflict of Interest, COI) 요약
정의 : 저자, 소속기관, 심사자, 편집인이 논문 작성 · 심사 · 출판 과정에 부적절한 영향을 미칠 수 있는 재정적 · 개인적 관계에 있는 경우
문제점 : 과학적 진실을 왜곡하고 학술적 판단(결정, 심사, 원고 작성)을 왜곡할 가능성 존재
대표적 예시
– 특정 제약회사로부터 연구비 지원받고 해당 회사 약품에 긍정적 결과 도출
– 심사 대상 논문이 경쟁 관계인 연구자의 것
– 편집인이 친분 있는 연구자의 논문을 특혜 심사
핵심 원칙 : 이해관계가 있을 경우 반드시 공개(Disclosure)해야 하며, 이를 통해 독자와 편집인이 연구 결과를 객관적으로 평가할 수 있도록 해야 함
- (성인간호학) 콩팥 요로계 건강문제와 간호 – 콩팥이식
- (성인간호학) 콩팥 요로계 건강문제와 간호 – 투석
- 신입 간호사가 일하는 것을 본 간호사의 표정
- (성인간호학) 콩팥 요로계 건강문제와 간호 – 신부전
- (성인간호학) 콩팥 요로계 건강문제와 간호 – 신생물